Presentazione di PowerPoint PowerPoint PPT Presentation
Title: Presentazione di PowerPoint
1
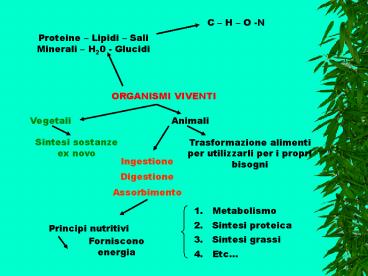
C H O -N
Proteine Lipidi Sali Minerali H20 - Glucidi
ORGANISMI VIVENTI
Animali
Vegetali
Trasformazione alimenti per utilizzarli per i
propri bisogni
Sintesi sostanze ex novo
Ingestione Digestione Assorbimento
- Metabolismo
- Sintesi proteica
- Sintesi grassi
- Etc
Principi nutritivi
Forniscono energia
2
ALIMENTI
Composti organici complessi
Elementi Minerali
Enzimi Succhi Gastrici
H20
Vitamine
Proteine
Sintesi
Glucidi
Lipidi
3
GLUCIDI
4
LIPIDI
Insolubili in acqua ma in solventi organici
cloroformio, benzene, etere, etc. Svolgono
funzioni di riserva di energia, contenuto di
energia paria 2,5 volte glucidi, si trovano nei
depositi adiposi (animali) e nei semi oleosi
(vegetali) Altre funzioni metabolismo membrane
cellulari, trasporto degli elettroni
5
Grassi
- Dal punto di vista alimentare sono i lipidi più
importanti, chimicamente costituiti da
trigliceridi (1 molecola di glicerina, in cui le
funzioni alcoliche sono esterificate da acidi
grassi) - I trigliceridi si differenziano per gli A.G che
entrano nella loro costituzione - Acidi grassi saturi (per il numero di atomi di
carbonio o per lassenza) - Acidi grassi insaturi (presenza di uno o più
doppi legami)
Gruppo carbossilico
Acido grasso
Glicerina
Grasso
Ctg idrocarburi
- La lunghezza della catena ed il N. di doppi
legami differenziano le proprietà chimico fisiche
degli A.G. - I doppi legami aumentano la reattività e
abbassano i punti di fusione - Il N. di atomi di C innalzano la T di fusione
- Animali A.G.S T. di fusione alta (grasso solido
a T a mò.). Essi sono in grado di sintetizzare
A.G.S e A.C.I a partire da carboidrati. Solo
alcuni insaturi integrati con dieta linoleico,
linolenico, arachidonico (AG essenziali funzioni
simili a quelle delle Vitamine, prevengono
disturbi dellaccrescimento, trofismo epiteliale,
efficienza riproduttiva) - Vegetali A.G.I, T fusione bassa (liquidi a T a
mò.)
6
Proprietà Grassi
Idrolisi o saponificazione produzione di saponi
(sali degli acidi grassi con sodio, potassio e
calcio Può essere prodotta artificialmente o
naturalmente per azione delle lipasi durante la
digestione dei trigliceridi
Ossidazione Gli A.G.I possono ossidarsi, infatti
latomo di C dei doppi legami può ossidarsi e
passare a Periossido prima e poi a Aldeidi o
Chetoni. Alterazione organolettiche e
nutrizionali dei grassi (irrancidimento dei
grassi nella conservazione dei foraggi).
Idrogenazione A.G.S vengono saturati per
aggiunta di atomi H agli atomi di C dei doppi
legami Usato dallindustria per la conservazione
degli alimenti grassi I batteri ruminali sono in
grado di idrolizzare prima e idrogenare poi i
grassi
7
Altri lipidi
Glicolipidi gruppo alcolico esterificato da uno
zucchero, presenti soprattutto nelle
erbe Fosfolipidi contengono fosforo, tra i
diversi fosolipi abbiamo le Leticine. Glico e
fosfolipidi svolgono importanti funzioni a
livello metabolico, fanno parte delle membrane
cellulari, dei tessuti nervosi e sono coinvolti
nel trasporto linfatico e sanguigno dei grassi
Altri lipidi non a base di glicerina, meno
importanti ma fondamentali
Sfingomieline e cerebrosidi contengono una base
azotata, la Sfingosina, si trovano nei tessuti
nervosi. Cere diffuse nel regno vegetale ed
animale, hanno funzione protettiva (no
nutrizionali, anzi sono indigeribili)
Steroidi importanti per la regolazione di alcune
funzioni metaboliche e digestive. Tra di essi il
colesterolo (costituente cervello, trasporto
ematico degli A.G, precursore della vitamina D e
acidi grassi biliari). Laccumulo eccessivo di
colesterolo nelle pareti dei vasi provoca la
arteriosclerosi Ormoni steroidei ormoni
femminili e maschili, il progesterone e i
corticosteroidi, importanti per la regolazione
del metabolismo degli zuccheri e dei grassi.
Terpeni regno vegetale, responsabili di alcuni
odori e sapori (limoni), nei pigmenti (clorofilla
e caroteni) e in alcune vitamine.
Prostaglandine diverse funzioni biologiche tra
cui sincronizzazione degli estri e induzione del
parto
8
PROTEINE
I principi alimentari più importanti, sono a
struttura quaternaria (H-O-C-N). 15 al 25 del
corpo animale, si trovano nei tessuti muscolari
(sostanze plastiche, poiché ogni organismo
accrescendosi produce nuove proteine). Si trovano
in tutte le cellule dove svolgono funzioni vitali.
Esistono infinite proteine, poiché esse sono
formate da una catena di amminoacidi, legati fra
loro in una sequenza particolare che designa una
proteina.
AMMINOACIDI
Costituiti da un gruppo amminico (-NH2) e uno
carbossilico (-COOH) che a sua volta è legato ad
un radicale libero che differenzia i vari
amminoacidi, per formare le proteine si legano
tra loro attraverso il legame peptidico, passando
da dipeptidi (2 amminoacidi, a polipetidi fino
alla formazione di proteine
Esistono circa 200 amminoacidi, ma quelli
essenziali sono 25 e 20 quelli più diffusi. Solo
i vegetali sono in grado di sintetizzare
amminoacidi ex novo a partire da azoto inorganico
(nitrati e ammoniaca) e da glucidi, gli animali
no, infatti devono utilizzare gli aminoacidi che
provengono dalla digestione di proteine.
Eccezione per i ruminanti, grazie alla flora
batterica possono farlo, ma non sintetizzano
tutti gli aminoacidi, mancano quelli essenziali.
9
CLASSIFICAZIONE AMMINOACIDI
Viene fatta in funzione dei radicali liberi che
li caratterizzano e a seconda del rapporto fra
gruppo amminico e carbossilico. Se nel radicale
sono presenti i primi allora lamminoacido sarà a
funzione basica, viceversa sarà acida. Quando
nessuno dei 2 è presente si avrà una funzione
neutra.
10
STRUTTURA DELLE PROTEINE
- Primaria data dalla sequenza degli amminoacidi
che contraddistingue ogni proteina - Secondaria dalla forma delle catene (spirale,
elica) rese stabili dai legami idrogeno dei
gruppi NH2 e CO del legame peptidico - Terziaria lelica si arrotola su stessa per
effetto di particolari legami fra i radicali
amminoacidi (ponti di solfuro, forze di Van der
Waal) - Quaternaria di alcune proteine complesse
costituite da più subunità proteiche che già
posseggono una struttura terziaria (tipiche di
alcune enzimatiche)
PROPRIETA DELLE PROTEINE
- Proprietà colloidali per la solubilità da nulla
(cheratine) a molto elevata (albumine) - Capacità di denaturazione processo in cui viene
modificata la struttura di una proteina, senza
modificare la sequenza amminoacidica, alterando
le proprietà chimiche, fisiche e biologiche (es.
inattivazione degli enzimi). Fonti calore (es
denaturazione dellalbume delluovo), acidi
forti, gli alcoli, lacetone, etc. Può in alcuni
casi essere reversibile, es precipitazione
soluzioni saline.
11
CLASSIFICAZIONE DELLE PROTEINE
- Proteine semplici protammine (sperma dei pesci)
istoni (costituzione delle emoglobine) che
unendosi agli acidi nucleici formano le
nucleo-proteine prolammine (semi di cereali)
gluteline (glutine frumento) albumine (siero,
latte, uova) globuline (siero del sangue, nel
latte, fibre muscolari et alii) scleroproteine
(struttura fibrosa, resistenti allidrolisi e
insolubili, sono esclusive del regno animale con
funzione meccanica e protettiva, come la
cheratina contenuta nei peli, piume, unghie, il
collagene presente nei vari tessuti connettivi e
fibroina della seta. - Proteine coniugate (oltre agli amminoacidi
contengono altre sostanze enzimi e ormoni)
fosfoproteine (caseina, ovovitellina)
cromoproteine (certi enzimi) glicoproteine
(mucine, mucoidi) lipoproteine (plasma
sanguigno, tuorlo duovo) nucleoproteine
(nucleo cellulare)
12
VITAMINE
Sono sostanze di composizione semplice e ben
definita, ma molto varia, presenti in
piccolissime quantità negli alimenti o
sintetizzabili dallorganismo di alcune specie
animali. Regolano i processi fisiologici degli
individui. Le vitamine hanno funzione catalitica,
cioè rendono possibili determinati processi
biochimici di ossidoriduzione, di assimilazione e
di sintesi. Generalmente le vitamine devono
essere assunte tramite gli alimenti.
CLASSIFICAZIONE DELLE VITAMINE LIPOSOLUBILI E
IDROSOLUBILI
Liposolubili sono solubilizzate solo da veicoli
grassi o da oli eterei
- Vit. A (retinolo) Si trova nei prodotti di
origine animale (latte, uova, etc.), nei vegetali
sottoforma di provitamine (carateni). Stimola la
crescita dei mammiferi e degli uccelli, protegge
gli epiteli dei vari organi. La carenza provoca
sviluppo stentato e gravi forme di diarrea negli
animali giovani. - Vit. D (ergocalciferolo, colicalciferolo)
scarsamente diffusa in natura (olio di fegato di
merluzzo, tonno, latte, uova, etc.). La D2 è
presente nelle erbe affienate in giornate di
forte insolazione. La D3 è sintetizzata dai
tessuti cutanei. Regola lequilibrio fra Ca e P,
favorisce la loro fissazione nel tessuto osseo.
La carenza provoca nei soggetti giovani
rachitismo, in quelli adulti osteomalacia
(decalcificazione con conseguente deformazione
delle ossa). - Vit. E (tocoferoli) possiede attività
antiossidante, è diffusa nel mondo vegetale,
specie nei germi di cereali (frumento, mais,
etc.). Esplica importanti funzioni inerenti la
fisiologia della riproduzione. - Vit. K (antiemorragica) abbondante nei foraggi
verdi e nel fegato dei suini. Raramente si
riscontra una carenza in campo zootecnico. E
utili alla sintesi della protrombina, sostanza
che interviene nella coagulazione del sangue .
13
IDROSOLUBILI soprattutto quelle del gruppo B
regolano il metabolismo, sono importanti nei
processi nutrizionali. Le carenze provocano minor
crescita, diminuzione dellappetito, alterazioni
articolari, cachessia (deperimento organico). Si
possono avere carenze nei soggetti giovani
(ruminanti, erbivori) suini, polli e nelluomo.
- Vit. B1 (tiamina o aneurina) diffusa in molti
tessuti vegetaliverdi. Stimola la funzione
digestiva, lattività cardiaca e muscolare,
regola la temperatura corporea. Non si ha carenza
nei bovini perché sintetizzata dai batteri
presenti nel rumine. - Vit. B2 (riboflavina, metabolismo acidi grassi),
B3,B6 (adermina, metabolismo proteico),B12,B13
(cobalamine, metabolismo proteicoutilizzazione
degli alimenti e sviluppo animali in
accrescimento), B14, assieme alla B1 formano le
vitamine del complesso B. - Vit. C (acido ascorbico) presente soprattutto
negli agrumi, interviene nei processi respiratori
della cellula. Antiscorbutica, una carenza
provoca emorragie della cute e delle gengive,
dimagrimento, astenia, dolori alle ossa e
giunture.
14
SALI MINERALI
Si trovano nellorganismo costituendo le ceneri,
si dividono in Macroelementi e Microelementi.
Essi sono indispensabili, una carenza può indurre
a diverse patologie, un eccesso può essere
ulteriormente dannoso poiché possono diventare
tossici.
Svolgono diverse funzioni plastica (costituzione
di vari tessuti e organi catalitica (entrano in
alcune reazioni del biochimismo cellulare.
Servono per regolare la pressione osmotica, la
permeabilità della membrana cellulare,
leccitatabilità neuro-muscolare, etc.
Tra alcuni minerali esiste linterdipendenza,
unalterazione di questa può produrre squilibri
metabolici. Una carenza può alterare la
produttività, laccrescimento. Controllo può
essere fatto attraverso la presenza di essi nel
profilo ematico. Esistono in commercio diverse
soluzioni (integratori minerali).
15
(No Transcript)
16
MACROELEMENTI
Calcio e Fosforo
Ca presente per il 98 nelle ossa, assicura la
coagulazione del sangue, regola leccitabilità
muscolare, lequilibrio acido-base del sangue,
ruolo importante nella coagulazione del latte,
funge da coenzima in diverse reazioni.
P si trova nello scheletro, nei tessuti, nei
liquidi corporei, costituente di varie molecole
(DNA, RNA, ATP, etc.), interviene nel metabolismo
di tutte le sostanze nutritive e
nellapprovvigionamento energetico della cellula,
interessa la fertilità.
Fabbisogni durante la crescita (formazione dello
scheletro), e negli adulti per il ricambio,
soprattutto nelle vacche lattifere, poiché parte
del calcio presente nello scheletro viene
mobilizzato per la secrezione del latte.
Assorbimento Ca (in forma non legata, poiché si
trova come carbonato, fosfato o ossalato) inizio
intestino tenue, mediato da una molecola
proteica. P (semi, frutti) viene assorbito nella
zona pilorico-duodenale, dipende dal pH
intestinale e dalla sua solibilità. Rapporto
21, nelle galline ovaiole 3/41 (formazione
del guscio uovo)
Carenze diminuzione contenuto ceneri nelle ossa
(rachitismo nei giovani e osteomalacia negli
adulti). Particolare importanza ha il collasso
puerperale (caduta del calcio a livello ematico)
nelle vacche subito dopo il parto. Manifestazioni
perdita di appetito, blocco della funzionalità
digestiva, paresi arti posteriori. Se non curato
coma e morte.
17
Magnesio 60 nelle ossa, influenza
leccitabilità muscolare, entra nella
costituzione di alcuni enzimi. Le diete non
manifestano quasi mai carenze. Eccessi di K,
acidi organici o acidi grassi liberi possono
inibire lassorbimento. Eccesso porta
alleliminazione del Ca (acque ipermagnesiache).
Sodio si trova nei liquidi (sangue, fluidi
extracellulare), regola i meccanismi di trasporto
attivo delle membrane cellulari e leccitabilità
muscolare. Aggiungere alla dieta sale
pastorizzato (NaCl), bisognare fare attenzione
quando nella dieta è somministrata la farina di
pesce.
Potassio si trova in abbondanza negli alimenti,
interviene nel metabolismo glucidico e proteico,
regola la pressione osmotica. Rapporto costante
con Na.
Cloro si trova come cloruro di sodio e di
potassio (sangue, cartilagini, stomaco),
raramente si verificano fenomeni di carenza.
Zolfo assunto con le proteine, si trova negli
alimenti sottoforma di solfati, superflua
laggiunta delle diete. Eccezione per la
produzione di lana e nella muta delle galline,
poiché piume e lana contengono proteine ricche di
amminoacidi solforati.
18
MICROELEMENTI
Ferro essenziale nella formazione
dellemoglobina, concentrato nel sangue.
Partecipa alla costituzione della mioglobina
(proteina che assicura la contrazione muscolare)
e di alcuni enzimi della respirazione cellulare.
Viene assorbito nel duodeno (ione ferroso), viene
immagazzinato nel fegato, nella milza e nel
midollo osseo. Carenze anemia. Somministrazione
per via parenterale (iniezioni sottocutanee o
endovenose).
Rame interagisce con altri elementi
oligodinamici, mobilizza le riserve di ferro,
entra nella costituzione di vari enzimi,
indispensabile nella sintesi dei pigmenti
melaninici. Carenze leccamento, imbianchimento
del pelame, disturbi di crescita. Fabbisogno
10/15 mg/Kg di ss. Dosi elevate effetto tossico.
Nei suini fino a 150 mg/Kg di mangime (effetti si
ripercuotono nelle feci).
Cobalto azione emopoietica (sintesi globuli
rossi), entra costituzione vitamina B12.
Manganese importante nella formazione dello
scheletro, necessario per lazione di alcuni
enzimi. Importante nellalimentazione del pollame
(schiusa uova, comparsa della perosi nei pulcini).
Molibdeno è contenuto negli enzimi che
presiedono al metabolismo delle purine. Altamente
tossico, inibisce lassorbimento del rame.
Selenio tossico a dosi elevate. Azione
antiossidante sinergica, stimola laccrescimento
e la fertilità. Carenze degenerazione muscolare
(distrofia muscolare, insufficienza del
miocardio).
19
Iodio essenziale per lattività della tiroide,
rare le carenze (crescita di animali deboli,
disturbi sessuali, comparsa del gozzo).
Fluoro presente nellacqua, nessun ruolo
nellalimentazione. Può essere tossico.
ACQUA
Il 50 70 del corpo è composta da acqua.
Essenziale per la vita degli esseri viventi,
poiché in essa avvengono tutte le reazioni
chimiche (potere solvente, mezzo di trasporto,
escrezione delle molecole). La quantità di acqua
nel corpo deve essere mantenuta costante (volume
cellulare, normale pressione osmotica. Le perdite
avvengono con la respirazione, con la
traspirazione, con le feci, con le urine e
secrezioni (latte, etc.). Assunzione tramite
abbeverata, recupero dagli alimenti solidi e
quella liberata dalle reazioni metaboliche. Le
esigenze variano tipo di animali, di alimenti e
dalle condizioni climatiche.
20
ENZIMI
Intervengono in tutte le reazioni chimiche
(processo digestivo, etc.). Svolgono unazione
catalitica, cioè aumentano la velocità della
reazioni, questo per le esigenze dovute alle
rapide trasformazioni che avvengono allinterno
del corpo. Sono altamente specifici, la
denominazione si ottiene aggiungendo la desinenza
asi alla reazione catalizzata e al substrato
coinvolto (es. enzimi che catalizzano lidrolisi
delle proteine appartengono alle idrolasi e più
specificatamente alle proteasi. Carenze no
reazione o insufficiente. Sono molecole proteiche
e la loro azione dipende dalla loro struttura. Il
molti casi non agiscono da soli, ma con un
cofattore o coenzima (elemento minerale o
vitamina) che si lega alla frazione proteica
(apoenzima) per attivarla.
ORMONI
Sono molecole di varia natura sintetizzate dalle
ghiandole endocrine e dai tessuti dellorganismo
e vengono immessi nel flusso sanguigno e
linfatico per raggiungere i vari organi, tessuti,
etc., per regolare e indirizzare lattività
metabolica. Azione fondamentale per il
coordinamento e lequilibrio delle funzioni
vitali, determinano la contrazione muscolare, la
secrezione ghiandolare, la maturità sessuale,
lequilibrio dei cicli sessuali e gravidanza, i
processi di crescita, di sviluppo e di
comportamento. Agiscono a concentrazioni
limitate, vengono rilasciati al momento del
bisogno e vengono inattivati una volta svolto il
lavoro. Somministrazioni per laccrescimento
(vietato dalla CEE).