1. dia - PowerPoint PPT Presentation
Title: 1. dia
1
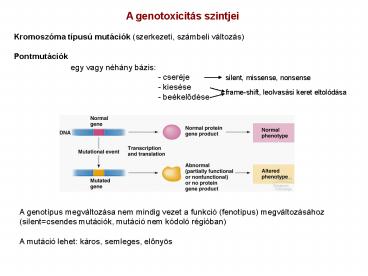
A genotoxicitás szintjei Kromoszóma típusú
mutációk (szerkezeti, számbeli változás) Pontmutá
ciók
egy vagy néhány bázis -
cseréje - kiesése - beékelodése
silent, missense, nonsense
frame-shift, leolvasási keret eltolódása
A genotípus megváltozása nem mindig vezet a
funkció (fenotípus) megváltozásához
(silentcsendes mutációk, mutáció nem kódoló
régióban) A mutáció lehet káros, semleges,
elonyös
2
Mutagén Karcinogén
- a mutagén fizikai vagy kémiai ágens, mely
növeli a mutációk képzodésének gyakoriságát - indukált mutáció a mutagének által okozott
változások a genetikai állományban - a halálozások oka a civilizált világban 40-ban
rákos daganat - - a rákos megbetegedések közel 90-át a
környezetünket szennyezo mutagének okozzák - - a mutagén vegyületek nagy része rákkelto
(karcinogén) is !!!!!!!!!!!! - - évente néhány ezer olyan vegyületet állítanak
elo, amelyek korábban nem léteztek a Földön
(gyógyszer alapanyagok, növény- vagy faanyagvédo
szerek, élelmiszer-adalék, kozmetikum, háztartási
vegyszer stb.) - a mutagének és a karcinogének közötti szoros
kapcsolat szükségessé teszi a környezetünkben
lévo mutagén vegyületek kimutatását
3
Spontán mutációk
- okai
- a bázisok alternatív formái (keto/enol,
amino/imino tautomerizáció) - a replikáció során a szálak elcsúszása
következtében kisméretu inszerciók és deléciók
keletkezése - - a DNS szerkezeti változásai (depurináció és
deamináció, amelyek a bázisok párosodási
tulajdonságait változtatják meg)
4
Tautomerizáció
Normál bázispárosodás (keto és amino formák)
Az adenin imino formája citozinnal, a guanin enol
formája pedig timinnel képes H-híd kialakítására.
A citozin imino formája adeninnel, a timin enol
formája pedig guaninnel képes H-híd
kialakítására.
A párosodási hiba a replikáció során az újonnan
szintetizált szálban megmarad és állandósul
5
- Indukált mutációk
- külso okokból származó mutációk
- vegyszerek számos módon okozhatnak mutációkat
- bázis analógok a DNS-be beépülnek, de nem a
megfelelo bázissal párosodnak - alkiláló, deamináló szerek, oxidáló anyagok a
DNS bázisok szerkezetét és párosodási
tulajdonságait megváltoztatják - interkaláló szerek a bázisok közé ékelodnek és
nukleotid inszerciót vagy deléciót okoznak
6
Bázis analógok
a természetes bázisokhoz hasonló szerkezetuek, a
DNS polimeráz a kettos spirálba beépíti
pl. 5-brómuracil (5BU) timin analóg adeninnel és
guaninnal is (!) képes párosodni tranziciót okoz
T-Agt5BU-Agt5BU-GgtC-G C-Ggt5BU-Ggt5BU-AgtT-A 2-amin
opurin (2AP) adenin analóg a timinen kívül
citozinnal is (!) képes párosodni tranziciót
okoz T-AgtT-2APgtC-2APgtC-G C-GgtC-2APgtT-2APgtT-A
7
Alkiláló szerek
alkil (-CH3, -CH2-CH3) csoportokat építenek a
nukleinsavak bázisaira és azokat módosítják
pl. etil-metánszulfonát (EMS) foként a guanint,
kisebb mértékben a timint módosítja a
6-etilguanin timinnel párosodik, ami C-GgtT-A
tranzíciót eredményez a 4-etil-timin a guaninnal
párosodik, és így T-AgtC-G tranzíció jön létre
8
Deamináló szerek a spontán deamináción kívül
különbözo vegyszerek is képesek a bázisok amin
csoportjait támadni
pl. salétromossav a citozint, az adenint és a
guanint támadja citozin uracil, mely a
következo replikáció során adeninnel párosodik és
C-G gt T-A tranziciót okoz adenin
hipoxantin, ami citozinnal párosodva T-A gt C-G
tranziciót eredményez guanin xantin, ez
elsosorban citozinnal, de kisebb mértékben
timinnel is párosodva C-G gt T-A tranziciót hoz
létre hidroxilamin a citozin amino csoportját
támadja, és hidroxilaminocitozin keletkezését
okozza a hidroxilaminocitozin adeninnel
párosodik, és C-G gt T-A tranziciót okoz
9
Interkaláló vegyületek
- általában gyurus vegyületek, melyek
térkitöltése a bázispárokhoz hasonlít - a DNS
kettos spirálban egymás melletti bázispár közé
képesek beépülni - a beépülés a kettos spirál
alakját torzítja, ami azután a replikáció során
egy nukleotid kiesését vagy beépülést
okozza pl. proflavin akridin sárga etidium-bromid
dioxin
10
A genotoxicitás mérése
- többféle, nemzetközileg elfogadott tesztrendszer
- bakteriális tesztek (Salmonella typhimurium,
Esherichia coli) - eukarióta egysejtuek (pl. Saccharomyces
cerevisiae, Aspergillus nidulans) - élesztogomba penészgomba
- rovarok (ecetmuslica Drosophila melanogaster)
- növények (lóbab, árpa, vöröshagyma)
- gerincessejt-vonalak (humán és egyéb emlos
sejtvonalak) - in vivo (egér, hörcsög, patkány)
11
Alternatív in vitro genotoxicitási tesztek
- állatkísérletek számának csökkentése
- gyors (short term study)
- - költséghatékony
- Végpontok
- pontmutáció
- DNS törés
- repair (DNS szintézis NEM az S fázisban)
- kromoszóma aberrációk
12
Mutációk detektálása
- - a fajok nemzedékrol nemzedékre mutatott
állandósága arra utal, hogy a mutációk
bekövetkezése ritka esemény - a valóságban azonban a megfigyelhetonél jóval
több mutáció keletkezik - mivel leggyakoribbak a recesszív mutációk, a
legtöbb új mutáció észlelését a dominancia
megakadályozza - az új mutációk észlelése ezért a legegyszerubb a
haploid szervezetekben - diploidokban a mutációk kimutatására speciális
rendszerek szükségesek - - a mutációk gyakorisága alacsony, ezért
mutánsokat nagy egyedszámú populációból kell
tudni kimutatni
13
Bakteriális reverz mutagenitási
teszt Kidolgozója, Bruce Ames után AMES
teszt Validált (OECD Guideline
471) Pontmutációk észlelésére alkalmas
Salmonella typhimurium apatogén, mutáns
törzseinek használatán alapul his-
mutánsainak reverzióját figyelik a tesztelendo
vegyületek hatására
Reverzió back mutáció
his Hisztidint szintetizál Hisztidinmentes
tápközegben életképes
his- Hisztidin bioszintézisére képtelen Csak
hisztidint tartalmazó tápközegben életképes
Nagy populációban bekövetkezo ritka mutációs
esemény detektálására alkalmas
14
Hisztidin bioszintézis
phosphoribosyl pyrophosphate
15
- A teszttörzsek jellegzetességei
- Különbözo típusú his mutációkat tartalmaznak,
ezért a mutáció reverziója történhet - bázispár szubsztitúcióval
- frame-shift segítségével
- különbözo hatásmechanizmusú mutagén vegyületek
mutathatók ki, azaz információt nyújt a - genotoxikus anyagok által eloidézett mutációk
típusáról
A tesztelo törzsek hibásak az excíziós
repairben uvr (érzékenyebb kimutatás,
epigenetikus ártalmak) LPS kialakításában rfa
(lipopoliszacharid bioszintézis, sejtfelszín), a
vizsgálandó anyag könnyebben jut be a sejtbe a
sejtfalon át
16
Salmonella baktériumok által képzett telepek
17
A kísérlet kivitelezése I.
S9 patkány májából készült enzimkivonat S9-et
adagolva modellezni lehet az emlosökben lezajló
enzimatikus reakciókat, így a bakteriális
géntoxikológiai tesztekbol következtethetünk a
szennyezoanyagok magasabb rendu szervezetekre
gyakorolt hatására
18
A kísérlet kivitelezése II.
19
Az eredmények értékelése
Egy vegyületre akkor mondjuk, hogy Ames-tesztben
nem mutagén, amennyiben legalább 4 törzsön
TA98, TA100, TA1535, TA97 és/vagy TA1537
bizonyította önmagában vagy S-9-es aktiválás
utáni hatástalanságát. Egyetlen törzsön mért
pozitív teszt esetén is mutagén a minosítés.
20
Továbbfejlesztett Ames teszt 96 lukú
mikrotitráló lemezen 6 törzzsel (TAMix) végezheto
egyszerre pH indikátor festék a tápközegben
(brómkrezol lila) A hisztidinmentes tápközegben
szaporodó (revertált) baktériumok savasítják a
tápközeget
21
RadarScreen
Saccharomyces cerevisiae Transzgenikus
élesztotörzs DNS fragmentációra aktiválódó
promoterriporter gén